Der Hofmannsche Zersetzungsapparat

Seit einer ganzen Weile sind alle Facharbeiten abgegeben. Meine war zur Elektrolyse von Wasser im Hofmannsche Zersetzungsapparat. Um den Versuch durchzuführen, benötigt man zwei Elektroden, in meinem Fall aus Platin, einer Spannungsquelle, einen Elektrolyten und natürlich einen Hofmannschen Wasserzersetzer.
Die Elektroden (1) werden unten in den Zersetzungsapparaten eingeführt, wodurch dieser an der Unterseite luftdicht verschlossen wird. Als nächstes werden die Ablaufventile (2) unten am Wasserzersetzer geschlossen und der Elektrolyt wird in den Hofmannschen Zersetzungsapparaten eingefüllt. Wenn der Pegel die Nullstriche links und rechts (4) auf der Skala erreicht, werden auch die oberen Ventile (5) geschlossen, wodurch das System luftdicht verschlossen wird.

Der Elektrolyt besteht aus verdünnter Schwefelsäure oder einer Salzlösung, welche benötigt wird, um die Leitfähigkeit des im Elektrolyten enthaltenen Wasser zu steigern. Da Wasser keine ausreichende Leitfähigkeit besitzt, um die Elektrolyse durchzuführen, ist der Einsatz eines Elektrolyten unerlässlich. Da die Ionen der Schwefelsäure oder der Salzlösung nur als Ladungsträger agieren, werden sie in der Reaktionsgleichung nicht erwähnt. Sie sind jedoch neben den Elektronen maßgeblich für die Menge der entstehenden Produkte verantwortlich.
Als nächstes wird die Elektrolyse gestartet. Dazu wird die mit den Elektroden verbundene Spannungsquelle (3) auf 12 V Gleichstrom eingestellt. Nach ca. 15 Minuten ist deutlich zu erkennen, dass sich auf beiden Seiten des Hofmannschen Zersetzungsapparaten Gas gebildet hat. Dabei ist das Volumen des Gases auf der Kathodenseite doppelt so groß, wie auf der Anodenseite.
Führt man mit dem auf der Kathodenseite entstandenen Gas die Knallgasprobe durch, stellt man fest, dass es sich bei dem entstandenen Gas um Wasserstoff handelt. Wenn man mit dem entstandenen Gas der Anodenseite die Glimmspahn-Probe durchführt, ergibt sich, dass es bei dem Gas um Sauerstoff handelt. Daraus resultieren folgende Reaktionsgleichungen:
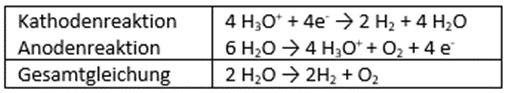
Bei der Elektrolyse von Wasser entstehen sowohl H2-Molküle als auch O2-Moleküle. Diese entstehen, da durch die zugeführte elektrische Energie die intermolekularen Bindungen im Wasser-Molekül beziehungsweise im Oxonium-Ion spalten, wodurch Wasserstoff und Sauerstoff frei werden. Die Elektrolyse ist damit eine Methode, um Stoffe mithilfe elektrischer Ladung zu trennen.